Bu sunuda 4. Ürogenital Kanserler Kongresi’nde yapmış olduğum “Testis Kanseri’nde Cerrahi Tedavi” başlıklı konuşmayı paylaşıyorum. Testis kanserinde cerrahi tedavi oldukça geniş bir konu olup, cerrahi tedaviyi Medikal ve Radyasyon Onkolojisi’nden bağımsız olarak detaylandırmak oldukça zordur. Bu nedenle bu sunuda cerrahi tedaviyi vakalar ve aldıkları tedavilerle birlikte değerlendirmek daha uygun olacaktır (slayt 2, slayt numaraları slaytların sağ alt köşesinde verilmiştir).
Birinci vaka sağ testiste 2 cm’lik kitle ile başvuran ve serum tümör belirteçleri normal olan 32 yasındaki bir hasta (slayt 3). Bu hastanın aynı zamanda testiküler mikrolitiazisi de bulunmaktaydı. Bu hastaya yaklaşım slayt 5’de özetlenmiştir. Testiste kitle ile gelen hastaya yaklaşımın temelini radikal orşiektomi operasyonu oluşturmaktadır. Ancak bu noktada önemli bir soru, bu genç hasta grubunda radikal orşiektomi’den hemen sonra aynı seansta testis protezinin yerleştirilip yerleştirilemeyeceğidir. Bu konuya ilişkin bir çalışmada 885 radikal orşiektomi yapılan hasta retrospektif olarak değerlendirilmiş ve testis protezi yerleştirilmesi önerilen 413 hastanın %52’si aynı seansta testis protezinin yerleştirilmesini tercih etmiştir (slayt 6). Hastanede kalış suresi ve planlanan haricinde hastane başvuru sayısı açısından (post-operatif 30 gün) her iki grup arasında fark saptanmamış ve yalnızca 1 hastanın protezi enfeksiyon nedeni ile çıkarılmıştır. Bu hali ile radikal orşiektomi ile eş zamanlı protez yerleştirilmesinin, güvenli ve hastaya önerilmesi gereken bir yaklaşım olduğunu söylemek yanlış olmaz.
Bu hastanın patolojisi klasik tipte seminom olarak saptanmış ve hastanın batın ve torakal görüntülemesinin normal olması nedeni ile hasta Evre 1 hastalık olarak tanı almıştır (slayt 7). Bu hali ile hastaya yaklaşımda, hastalığın bu evresinde izlem, kemoterapi ve radyoterapi seçenekleri bulunmaktadır. Bu evredeki hastaya, metastatik testis tümörünün cerrahi tedavisinin temelini oluşturan retroperitoneal lenf nodu diseksiyonu (RPLND) gerekmemektedir. Radyoterapi de, bu genç hasta grubunda ikincil kanser gelişimi ile ilişkili olduğundan önerilmez. Bu haliyle izlem veya kemoterapi seçenekleri arasından bir secim yapmak gerekmektedir. Bu noktada tedavi kararını verirken, Evre 1 seminomlar için kullanılan prognostik risk faktörleri devreye girmektedir (slayt 8). Bu risk faktörleri tümörün 4 cm’den büyük olmasi ve rete testis invazyonudur. Eğer bu risk faktorlerinden ikisi varsa, hastalar tek doz karboplatin kemoterapisi almakta, eger risk faktoru bulunmuyorsa hastalar periyodik aralıklarla takip edilmektedir. Tek risk faktörü olanlarda, yaklaşım net olmayıp, hastanın ve hekimin tercihine göre karar verilmektedir. Yukarıda bahsedilen hasta tek doz kemoterapi almıştır (slayt 9).
Testis tümörü bulunan hastalardaki önemli bir konu da fertilite değerlendirmesidir (slayt 11). Genel olarak bu grup hastaların yaklaşık olarak %40-50’sinde altta yatan fertilite problemi bulunduğundan hastanın fertilite potansiyelinin radikal orşiektomi öncesinde değerlendirilmesi ve sperm kriyoprezervasyonu büyük önem taşımaktadır. Bunun icin tum hastalara semen analizi yapılmalı ve bunun yanında hastanın fertilite ve testis fonksiyonu açısından temel hormonal parametreleri (total testosteron, LH, FSH) değerlendirilmelidir.
Ayrıca bu vakada testikuler mikrolitiazis olduğu radyoloji raporunda bildirilmişti. Benzer durum sağlıklı popülasyonda nadir olmayarak karşımıza çıkmaktadır. Bizim bu konudaki deneyimimize göre diffuz testiküler mikrolitiazis (ultrasonografide yıldızlı gökyüzü manzarası), testis tümörü açısından risk faktörü oluşturmakta ve özellikle hastada kriptorsidizm, hipopadias, subfertilite veya infertilite gibi testikuler disgenezis sendromunun komponentleri de varsa; bu hastalara yıllık Üroloji muayenesi ile birlikte testiküler ultrasonografi önerilmedir (slayt 13, 14).
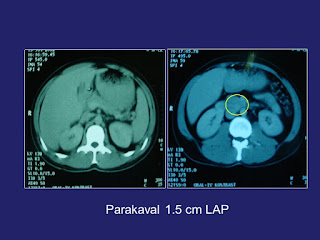
Vakaya devam edersek, eğer bu hastada 2 cm bir retroperitoneal bir lenf nodu tespit edilseydi, artik Evre 2 olan bu seminom vakasında tedavi yaklaşımımız nasıl olurdu? Bu haliyle hastanın temel tedavisi radyoterapidir (slayt 16). Hastaya testis tümörünün bulunduğu tarafa hokey sopası tarzında ipsilateral radyoterapi (evre 2a olduğu için 30 Gy) uygulanması gerekmektedir. Evre 2b yani kitle boyutu 2-5 cm olan hastalarda 36 Gy radyoterapi uygulanırken, evre 2c hastalıkta genel olarak 3 kür BEP veya eğer Bleomycin konusunda çekinceler varsa, 4 kür EP verilmektedir. Kemoterapi kararını verirken, özellikle 3 cm’den küçük kitleler konusunda vital tümör dokusunun tanınmasında önemli bir tanı aracı olan FDG PET-CT’den faydalanılabilir.
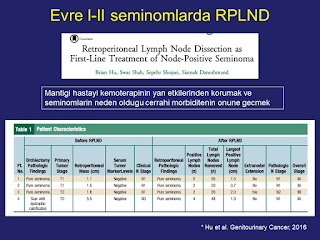
Ancak son yıllarda bu grup hastayı kemoterapinin yan etkilerinden korumak ve kemoterapinin neden olacağı ve ameliyatı güçleştiren dezmoplastik reaksiyon gelişmeden önce RPLND yapmak konusunda da görüşler bildirilmektedir (slayt 17, 18). Bu konuda küçük bir vaka serisinin analizi ile birlikte mevcut literatürün değerlendirildiği bir makalede opere edilen hastaların hiçbirisinde relaps saptanmazken, hastalardan 25-55 arası lenf nodu çıkarılmıştır. Ayrıca alternatif yöntemler olan radyoterapi, kemoterapi veya her ikisinin kombinasyonuna benzer hatta bir miktar daha iyi sonuçlar elde edilmiştir. Vaka sayısının azlığı nedeni ile henüz yeterince değerlendirilememiş olan Evre 2 seminom hastalarında RPLND yaklaşımı, RPLND’nin getireceği cerrahi morbidite de göz önüne alındığında, henüz standart bir yöntem olmaktan çok uzaktır.
İkinci vaka 37 yaşında ve sol testiste ele gelen sertlik nedeni ile başvuran bir hasta. Hastaya yapılan skrotal ultrasonografide 3 cm çapında solid kitle saptanmış ve hastanın her iki tumor belirteci de yüksek (slayt 19) olarak saptanmıştır. Diğer önemli bir nokta da; hastanın diğer testisinin hipoplazik ve hacminin de yaklaşık olarak 10 cc olmasıdır.
Bu aşamada hastaya organ koruyucu cerrahinin önerilip önerilemeyeceği önemli bir konudur. Organ koruyucu cerrahinin güncel endikasyonları slayt 21’de verilmiştir. Ancak bu yaklaşım önerilirken, testisin geriye kalan kısmında da; yüksek oranda germ cell neoplasia insitu (GCNIS) bulunabileceği ve testisin geriye kalan kısmının bu nedenle radyoterapi alabileceği bilinmelidir. Bu konudaki önemli çalışmalardan birisi ülkemizde çok merkezli olarak gerçekleştirilmiştir (slayt 22). Bu çalışmanın verilerine göre tümör boyutu arttıkça, çıkarılan kitlenin malign olma ihtimali artmakta ve buna paralel şekilde GCNIS bulunma olasılığı da artmaktadır.
Yeri gelmişken, GCNIS için kontrlateral testis biyopsisi yapılmasının endkasyonlarını da hatırlatmakta fayda vardır (Slayt 23). Genel olarak yapılan çalışmalarda, karşı taraf testiste %9’a varan oranlarda görülen GCNIS, testis volümünün 12 cc’den düşük olması, kriptorsidizm veya kotu spermatogenez varlığında yapılmalıdır. Tespit edildiğinde de temel tedavisi radyoterapidir. Hastanın final patolojisi slayt 24’de verilmiştir.
Seminomda olduğu gibi evre 1 non-seminamatöz hastalıkta da prognostik risk faktorlerinin degerlendirilmesi, tedavi kararını vermede büyük önem taşımaktadır. Bu risk faktörleri ile birlikte tedavi alternatifleri ve bunların avantajları ve dezavantajları slayt 27 ve 28’de verilmiştir. Bu hastada vasküler invazyon bulunmadığı ve embriyonel karsinom oranı %10 olduğu için hastaya izlem tedavisi önerilmiştir. Evre 1 NSGCT’de primer RPLND hastalığın evrelemesini en iyi yapan yöntem olmasına karşın, cerrahinin yarattığı morbidite kemoterapi rejimlerinin popülarite kazanmasına neden olmuştur. Bu konuda yapılmış randomize kontrollü bir çalışmada tek doz kemoterapi, primer RPLND’ye göre 2 yıllık nükssüz sağkalım açısından “intent to treat” popülasyonda yaklaşık olarak %7 avantajlı olarak bulunmuştur (slayt 28). Ancak bu çalışmanın kısa takip suresi ve lenfadenektomi sınırlarının standardize edilmemiş olması temel eleştiri noktalarını oluşturmaktadır.
Vakaya devam edersek (slayt 29), post-operatif dönemde normal seviyelere inmiş olan tümör belirteçleri, operasyonun 6. ayında yükselmiş ve batin görüntülemesinde paraaortic alanda 1 cm ve 7 mm’lik 2 adet lenf nodu tespit edilmiş. Bu durumda hastanın tedavisi tüm tümör belirteçleri yüksek olan hastalarda olduğu gibi kemoterapidir ve hasta 3 kur BEP tedavisi alacaktır. Burada önemli nokta evre 2 hastalık için en etkili tedavinin kemoterapi ve RPLND kombinasyonu olduğunun bilinmesidir. Evre 2 hastalıkta kemoterapi sonrası rezidüel kitlelerin tedavisindeki temel cerrahi yöntem RPLND’dir. Orsiektomi sonrası tümör belirteçleri negatif olan hastalar için algoritma slayt 31’de verilmiştir.
Retroperitoneal lenf nodu diseksiyonunun doğru ve yeterli yapılabilmesi için sağ ve sol testis tümörlerinin lenfatik yayılımının bilinmesi gereklidir (slayt 32). Sağ testis tümörleri temelde interaortokaval lenf nodlarına yayılmaktadır. Bunun yanında precaval, parakaval, retrocaval ve ayni taraf ilyak lenf nodlarinda da tutulumlar meydana gelebilmektedir. Sağ taraf tümörler, sol tarafa göre; daha fazla karşı testisin yayılım alanlarına metastaz yapma özelliği göstermektedirler. Sol testisten kaynaklanan tümörlerse daha çok, preaortic, paraaortic, retroaortic ve ayni taraf ilyak lenf nodlarına yayılım gösterirler.
RPLND operayonu denilince tek tip bir operasyon akla gelmemelidir. Yapilma amacina gore birden fazla tipi vardır (slayt 33). Ancak en sık yapılan tipi modifiye şablon RPLND’dir (slayt 34). RPLND operasyonu açık, laparoskopik veya robotik tekniklerle yapılabilmektedir. Istanbul Tip Fakultesi’nde de 40 yılı aşkın bir suredir yapılan bu operasyonlar zaman içerisinde uygun vakalarda laparoskopik cerrahi yönünde evrim göstermiştir. Slayt 36’da iki taraflı RPLND’nin operasyon sırasındaki görüntüsü görülmektedir. Buna göre bu operasyonun sınırlarını üstte sol renal ven, lateralde üreterler, distalde ise her iki ilyak bifurkasyon oluşturmaktadır. Bu operasyon teknik olarak testis tümörünün yayılım alanlarının hemen hemen tamamını kapsamasına karşın, oldukça morbid bir operasyon olup; başta ejakulatuvar disfonksiyon olmak üzere önemli komplikasyonlarla ilişkilidir. Bu nedenle zaman içerisinde çoğunlukla yerini modifiye şablon RPLND’ye bırakmıştır. RPLND tüm batını ilgilendiren bir operasyon olduğundan slayt 37’deki gösterilen vakada olduğu gibi komplike lezyonlarda multidisipliner bir cerrahi yaklaşımı gerektirmektedir. Çoğu zaman operasyonun ilgili kısımlarında genel cerrahi ve kalp ve damar cerrahisinden meslektaşlarımız dahil olmaktadır. Burada temel amac geride metastatik kitle veya nüks etme potansiyeli bulunmayan bir lenf nodu bırakmamaktadır.
Günümüze kadar RPLND’nin etkinliği Evre 2 hastalarda pek çok çalışma ile değerlendirilmiştir. Klasik bir açık cerrahide, slayt 38’de verilen derleme makalesinde görüldüğü üzere; unilateral şablonda hastalığın nüks etme ihtimali %6.3, bilateral şablonda %14.6 ve şablon ayrımı yapılmadan yapılan analizde ise; %11.2 olarak saptanmıştır (slayt 38). Laparoskopik ve robotik cerrrahi gibi minimal invazif tedavi yöntemlerinde bu oranlar sırası ile %2.1, %3.5 ve %7.8 olarak saptanmıştır (slayt 39). Ancak minimal invazif yöntemlerin genel olarak daha düşük tümör yükü olan hastalarda uygulandığını belirtmek gerekir.
RPLND sırasında diseksiyonun unilateral mi; yoksa bilateral mi yapılacağını göstermede önemli bir yol gösterici Heidenreich kriterleri’dir (slayt 40). Buna göre, interaortokaval lenf nodlarının varlığında ve/veya 5 cm’den büyük lenf nodlarının varlığında bilateral diseksiyon yapılmalıdır. Bu kriterlerin değerlendirildiği bir validasyon çalışmasında, bu kriterlerin doğru evrelemedeki etkinliği %100 olarak saptanmıştır.
Slayt 41 ve 42’de son dekadda Ürolojik cerrahinin kalbine yerleşmiş olan robotik cerrahinin etkinliği gösterilmiştir. Buna göre robotic cerrahinin kısa dönemdeki etkinliği hem primer, hem de kemoterapi sonrası RPLND için açık cerrahi ile benzerdir. Ancak orta ve uzun donemdeki sonuçları henüz tatminkar düzeyde rapor edilmemiştir.
İşaret edilmesi gereken önemli bir konu da etkin bir cerrahi için tecrübenin çok önemli olduğudur. Bu konuda yapılan bir çalışmada (slayt 43), yılda 5 taneden daha az RPLND yapan kliniklerin başarısının, bu rakamdan daha fazla RPLND yapan kliniklerden daha kotu olduğu bildirilmektedir. Bu konuya işaret eden daha pek çok çalışma kaleme alınmıştır. RPLND Üroloji disiplininde yapılan en kapsamlı cerrahilerden birisi olup lenfosel, ileus, üreter yaralanması, intraoperative kanama gibi, pek çok ve ciddi komplikasyonlarla ilişkidir (slayt 44). Komplikasyonlar açısından klasik cerrahi yöntemler ile minimal invazif yöntemler arasında belirgin bir fark bulunmamaktadır. Slayt 45 RPLND konusunda tecrübenin önemine işaret etmektedir.
RPLND’nin belki de en rahatsız edici komplikasyonu ejdakulatuvar disfonksiyon’dur ve genel olarak kendisini “kuru boşalma” olarak göstermektedir. Bu komplikasyon büyümüş olan retroperitoneal lenf bezlerinin diseksiyonu sırasında, T12-L4 arasındaki post-ganglionik sempatik liflerin veya aortun ön yüzünden kaudale doğru seyreden hipogastrik pleksusun zarar görmesi nedeniyle oluşmaktadır. Unilateral şablonların geliştirilmesinin nedeni de; bu can sıkıcı komplikasyonun önüne geçebilmektir (slayt 46). Bunun yanında iki taraflı diseksiyonun gerektiği durumlarda, post-ganglionik sempatik lifleri korumak için sinir koruyucu RPLND teknikleri de geliştirilmiştir.
İstanbul Tip Fakültesi’nin RPLND konusundaki deneyimi slayt 47’de verilmiştir. Buna gore ortalama takip suresi 5 yıl olan 94 hastada, nüks oranı %5.6 olarak saptanmış ve 5 yıllık kansere özgü sağkalim %94.6 olarak tespit edilmiştir. Bu hastaların %91.5’inde ejakulatuvar fonksiyon korunmuştur.
Bu slayttan sonraki vakalar ileri evre ( Evre 2c) metastatik testis tümörlerinde cerrahi yaklaşımın gözden geçirilmesi amacı ile verilmiştir. Tüm vakaların ortak noktası temel tedavilerinin kemoterapi ve ardından RPLND olmasıdır. Bu vakalar için tartışma konularından yalnızca birisi özellikle önem taşımakta ve RPLND konusundaki geleneksel tartışma konularından birisini oluşturmaktadır. Buna göre kemoterapi sonrası retroperitoneal kitle boyutu 1 cm olan hastalara nasıl yaklaşılacağı belirsizliğini korumaktadır. Bu konudaki geleneksel yaklaşım hastalık nüks ederse RPLND operasyonu önermektir. Bu konuda yapılan bir metaanaliz de bu yaklaşımı doğrular niteliktedir (slayt 51). Buna göre, kemoterapi sonrası, retroperitoneal kitleleri bu boyutlara inen ve RPLND yapılan hastaların nüks oranları yalnızca izlenen hastalardan farklı değildir. Bu çalışmanın verilerine göre bu grup hastaların %97’sine RPLND gerekmemektedir.
Sonuçta yukarıda detaylandırmaya çalıştığım bu sunuda mümkün olduğu kadar kısa ve anlaşılır şekilde testis tümörlerinin cerrahi tedavisini özetlemeye çalıştım. Umarım bu satırları okuyan meslektaşlarım bu sunudan faydalanırlar. Böylece emek gerektiren bu sununun hedefi beklenenin ötesine geçer.